Le dipôle électrostatique
Voici une expérience toute simple, qui met en lumière la force électrostatique, et l'influence qu'elle a sur l'eau. Nous allons expliquer ici comment la force électro-statique peut s'exercer sur de l'eau, car ça n'est pas si évident.
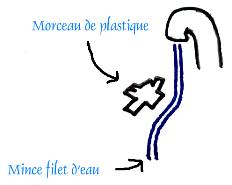 | Frottez un sac plastique contre votre pull (en laine de préférence), et approchez le d'un mince filet d'eau. Si vous avez correctement frotté le sac plastique, vous allez voir que le filet d'eau est dévié, sans être en contact avec le sac, bien sûr. |
Le sac plastique était chargé, ce qui explique qu'il ait crée un champ électrique. Mais est-ce que l'eau était chargée, elle ? La réponse est non, car l'eau est constituée d'atomes, qui comportent autant de charges positives que de charges négatives. Une molécule d'eau est donc neutre. Mais on est forcés de constater qu'une molécule, même neutre, n'est pas insensible au champ électrique. On va voir pourquoi.
De façon générale, les atomes sont effectivement neutres, en ce sens que la somme des charges des particules qui les composent fait zéro. Mais individuellement, chaque électron reste sensible au champ électrique. De même, le noyau y est sensible : il est positif, et constitué de protons soudés entre eux par une force plus grande que la force électrique (sinon, ils se repousseraient entre eux). Si on met un atome dans un champ électrique, les électrons seront attirés d'un côté, et le noyau de l'autre, puisqu'ils ont des charges différentes.
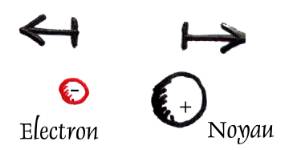 | Ici, on voit que soumis à un même champ électrique (dirigé vers la droite), le noyau, chargé + va vers la droite, tandis que l'électron est attiré dans la direction opposée, car il a une charge négative. Au final, l'électron est plutôt à gauche, le noyau plutôt à droite, on a un dipôle électrostatique. |
On en arrive à dire du coup qu'un côté de l'atome est plus négatif (le côté duquel les électrons sont attirés), alors que l'autre est plus positif. On dit que l'atome s'est polarisé. On a ce qu'on appelle un dipôle électrostatique. Et si un dipôle est globalement neutre, il n'est pas pour autant insensible au champ électrique. Il est attiré par les zones où le champ électrique est fort, donc autant par les charges positives que négatives ! Et de plus, il crée lui-même un champ électrique, qui n'est pas très grand, parce que le dipôle est globalement neutre, mais qui n'est pas nul. Et par exemple, ce champ peut du coup transformer un autre atome en dipôle aussi, etc... Du coup, deux atomes s'attirent forcément, même s'ils sont neutres, parce qu'ils peuvent se comporter comme des dipôles.
Pour vous donner une idée un peu plus précise de la façon dont se comporte un dipôle, il suffit de vous parler d'aimants : les aimants sont aussi des dipôles, mais des dipôles magnétiques, pas électro-statiques. Les aimants s'attirent parce qu'ils sont attirés par les champs forts (à condition d'être bien orientés).
Le champ électrique a donc une influence, même sur des atomes, qui sont neutres. Les atomes en effet sont constitués de particules chargées, qui sont toujours sensibles au champ électrique. Ils forment donc des dipôles, et sont attirés par les zones de champ fort. Comme ils créent aussi un champ électrique, les atomes s'attirent ainsi les uns les autres. Et c'est ce qui explique toutes les interactions entre molécules, et donc comment fonctionnent les cellules, pourquoi l'eau peut être sous plusieurs états (liquide, solide, gaz), et pas que l'eau d'ailleurs. Bref, c'est essentiel, au point qu'on a donné un nom à ces forces interatomiques ou intermoléculaires : les forces de Van der Waals.
Pour revenir à l'eau, l'eau se comporte comme un dipôle, car l'oxygène attire les électrons plus que l'hydrogène. Donc le côté de l'oxygène est plus négatif, et le côté de l'hydrogène plus positif. Elle est attirée donc par les zones de champ fort, donc autant par des charges positives que par des charges négatives. C'est pour cela que le jet d'eau est courbé : les molécules d'eau sont attirées par les charges présentes sur le sac.